CellCept® 500 mg Filmtabletten (Chargen E0278B01, E0456B01, E0458B01, E0462B01, E0469B01, E0479B01, E0480B01, E0484B01, E0487B01, E0489B01, E0497B01, E0502B01, E0504B01, E0507B01, E0512B01, E0513B01, E0519B01, E0533B01, E0545B01, E0546B01, E0548B01, E0556B01, E0565B01, E0575B01, E0576B01): Fälschungen auf dem legalen deutschen Markt angeboten
22.06.2018
Wirkstoff: Mycophenolatmofetil
Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) weist auf den Abschluss der Untersuchungen zu bestätigten gefälschten Chargen des Arzneimittels CellCept® 500 mg Filmtabletten der Firma Roche Registration Limited hin, die in Deutschland in Apotheken und bei Großhändlern entdeckt wurden. Das Arzneimittel enthält regulär den Wirkstoff Mycophenolatmofetil und wird in Kombination mit Ciclosporin und Corticosteroiden zur Prophylaxe von akuten Transplantatabstoßungsreaktionen bei Patienten mit allogener Nieren-, Herz- oder Lebertransplantation angewendet.
Sieben weitere mittels Laboranalyse bestätigte gefälschte Chargen sind nun bekannt. Die Chargen sind real existierende Chargen, die in 50er bzw. 150er Packungsgröße landesspezifisch für einzelne Länder (Niederlande, Frankreich, Belgien) zertifiziert wurden.
- E0456B01 (Verfalldatum 01/2020), im Original in französischer Aufmachung für den französischen Markt bestimmt
- E0462B01 (Verfalldatum 01/2020), im Original in französischer Aufmachung für den französischen Markt bestimmt
- E0480B01 (Verfalldatum 02/2020), im Original in belgischer Aufmachung für den belgischen Markt bestimmt
- E0487B01 (Verfalldatum 02/2020), im Original in niederländischer Aufmachung für den niederländischen Markt bestimmt
- E0489B01 (Verfalldatum 02/2020), im Original in französischer Aufmachung für den französischen Markt bestimmt
- E0502B01 (Verfalldatum 03/2020), im Original in belgischer Aufmachung für den belgischen Markt bestimmt
- E0533B01 (Verfalldatum 04/2020), im Original in französischer Aufmachung für den französischen Markt bestimmt
Die Chargen wurden illegal umverpackt und sind in deutsch-niederländisch-österreichischer Aufmachung (Packungsgröße 150 Stück) auf den deutschen Markt gebracht worden.
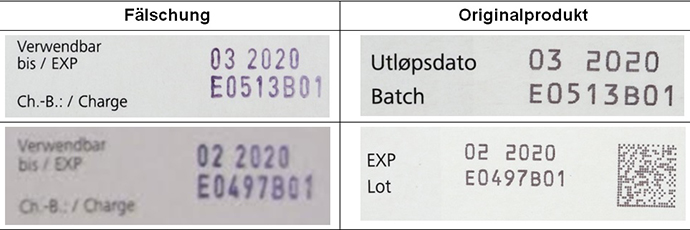
Untersuchungen der Firma Roche ergaben, dass die deutsch-niederländisch-österreichischen Faltschachteln (Packungsgröße 150 Stück) in allen Fällen gefälscht sind. Die untersuchten Blister und Filmtabletten entsprechen der Identität des Originalproduktes. Die Fälschungen sind, wie die vorherigen bestätigten Fälschungen, anhand der Druckfarbe der variablen Daten auf den Faltschachteln (Fälschung lila bzw. blau, Original schwarz), zu identifizieren.
Die Untersuchungen der erhaltenen Reklamationsmuster durch die Firma Roche sind abgeschlossen. Eine Übersicht aller berichteten Chargen ist Anhang 1 zu entnehmen.
Die Herkunft der Fälschungen ist inzwischen bekannt, strafrechtliche Maßnahmen gegen die Fälscher wurden entsprechend initiiert. Dennoch kann nicht ausgeschlossen werden, dass noch weitere Chargen betroffen sind. Sicher ist, dass die Fälschungen auf den deutschen Markt gelangt sind.
Das BfArM steht in engem Kontakt mit den Landesbehörden, die in Deutschland für die Überwachung des Verkehrs mit Arzneimitteln zuständig sind, und der Europäischen Arzneimittelbehörde EMA. Sollten weitere wichtige Informationen vorliegen, wird das BfArM unverzüglich darüber informieren. Daher weist das BfArM Großhändler, Apotheker und Anwender darauf hin, die Farbe des Aufdrucks der Faltschachtel sowohl bei diesen, wie auch bei anderen Chargen des Arzneimittels zu prüfen und Verdachtsfälle dem BfArM zu melden.
Anhang 1 - Übersicht aller berichteten Fälschungen in Deutschland
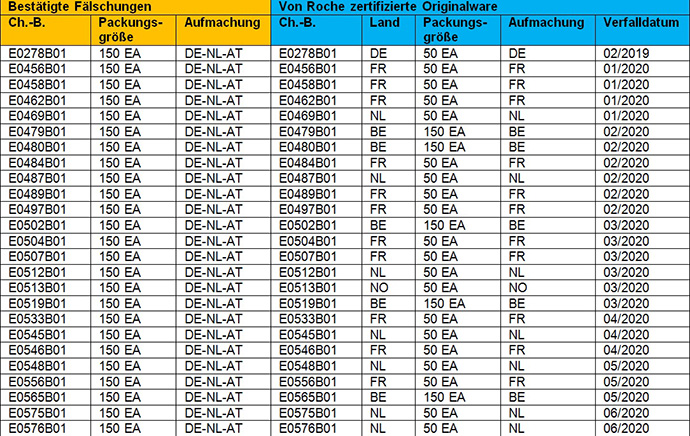
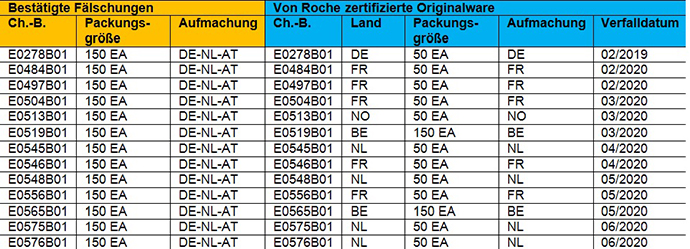
1) Bestätigte Fälschungen - CellCept 500 mg Filmtabletten Chargen (25)
Die Original Roche landesspezifische Aufmachung (für Frankreich, Belgien, die Niederlande oder Norwegen) ist nicht in Deutschland verkehrsfähig oder die landesspezifische Aufmachung für Deutschland (E0278B01) wurde nicht in der 150er Packungsgröße für den deutschen Markt zertifiziert.
Bestätigte Fälschung, 150er Packungsgröße, 3-Länderaufmachung (DE-NL-AT); Blister und Filmtablette entsprechen der Identität des Originalproduktes.
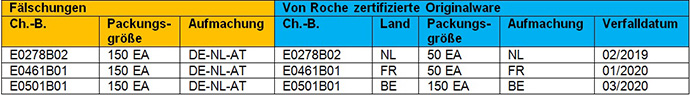
2) Fälschungen (keine Tablettenprobe verfügbar) - CellCept 500 mg Filmtabletten Chargen (3)
Die Original Roche Aufmachung ist entweder nicht in Deutschland verkehrsfähig oder wurde nicht in der 150er Packungsgröße für den deutschen Markt zertifiziert.
Reklamationsmuster stehen nicht für Untersuchung zur Verfügung, die Aufmachung zeigt jedoch eine Fälschung an.
Ergänzung vom 18.04.2018 (Chargen E0513B01, E0497B01)
Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) weist erneut auf Fälschungen des Arzneimittels CellCept® 500 mg Filmtabletten der Firma Roche Registration Limited hin, die in Deutschland in Apotheken und bei Großhändlern entdeckt wurden. Das Arzneimittel enthält regulär den Wirkstoff Mycophenolatmofetil und wird in Kombination mit Ciclosporin und Corticosteroiden zur Prophylaxe von akuten Transplantatabstoßungsreaktionen bei Patienten mit allogener Nieren-, Herz- oder Lebertransplantation angewendet.
Gefälschte Arzneimittel wurden mit den im Folgenden aufgeführten Chargen-Bezeichnungen identifiziert. Die Chargen sind real existierende Chargen, die in 50er bzw. 150er Packungsgröße landesspezifisch für einzelne Länder (Niederlande, Frankreich, Norwegen, Belgien, Deutschland) zertifiziert wurden.
- E0278B01 (Verfalldatum 02/2019), im Original in deutscher Aufmachung für den deutschen Markt bestimmt
- E0484B01 (Verfalldatum 02/2020), im Original in französischer Aufmachung für den französischen Markt bestimmt
- E0497B01 (Verfalldatum 02/2020), im Original in französischer Aufmachung für den französischen Markt bestimmt
- E0504B01 (Verfalldatum 03/2020), im Original in französischer Aufmachung für den französischen Markt bestimmt
- E0513B01 (Verfalldatum 03/2020), im Original in norwegischer Aufmachung für den norwegischen Markt bestimmt
- E0519B01 (Verfalldatum 03/2020), im Original in belgischer Aufmachung für den belgischen Markt bestimmt
- E0545B01 (Verfalldatum 04/2020), im Original in niederländischer Aufmachung für den niederländischen Markt bestimmt
- E0546B01 (Verfalldatum 04/2020), im Original in französischer Aufmachung für den französischen Markt bestimmt
- E0548B01 (Verfalldatum 05/2020), im Original in niederländischer Aufmachung für den niederländischen Markt bestimmt
- E0556B01 (Verfalldatum 05/2020), im Original in französischer Aufmachung für den französischen Markt bestimmt
- E0565B01 (Verfalldatum 05/2020), im Original in belgischer Aufmachung für den belgischen Markt bestimmt
- E0575B01 (Verfalldatum 06/2020), im Original in niederländischer Aufmachung für den niederländischen Markt bestimmt
- E0576B01 (Verfalldatum 06/2020), im Original in niederländischen Aufmachung für den niederländischen Markt bestimmt
Die Chargen wurden illegal umverpackt und sind in deutsch-niederländisch-österreichischer Aufmachung (Packungsgröße 150 Stück) auf den deutschen Markt gebracht worden.
Untersuchungen der Firma Roche ergaben, dass die deutsch-niederländisch-österreichischen Faltschachteln (Packungsgröße 150 Stück) in allen Fällen gefälscht sind. Die untersuchten Blister und Filmtabletten entsprechen der Identität des Originalproduktes. Die Fälschungen sind anhand eines eindeutigen Kriteriums, der Druckfarbe der variablen Daten auf den Faltschachteln (Fälschung lila bzw. blau, Original schwarz), zu identifizieren (siehe Abbildungen).
Packungen mit den Sicherheitsmerkmalen "Serialisierungsnummer, Manipulationsschutz mit Hologramm" sind nicht betroffen.
Die Untersuchungen sind noch nicht abgeschlossen. Eine Übersicht aller bisher berichteten Chargen ist Anhang 1 zu entnehmen. Es kann daher nicht ausgeschlossen werden, dass noch weitere Chargen betroffen sind.
Die Herkunft der Fälschungen wird untersucht. Sicher ist, dass die Fälschungen auf den deutschen Markt gelangt sind. Das BfArM steht in engem Kontakt mit den Landesbehörden, die in Deutschland für die Überwachung des Verkehrs mit Arzneimitteln zuständig sind, und der Europäischen Arzneimittelbehörde EMA. Sobald weitere Informationen vorliegen, wird das BfArM unverzüglich darüber informieren.
Das BfArM weist Großhändler, Apotheker und Anwender darauf hin, die Farbe des Aufdrucks der Faltschachtel sowohl bei diesen, wie auch bei anderen Chargen des Arzneimittels zu prüfen und Verdachtsfälle dem BfArM zu melden.
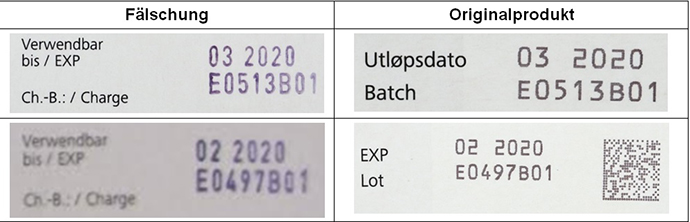
Foto der Fälschungen in deutsch-niederländisch-österreichischer Aufmachung und des Originalproduktes (norwegische bzw. französische Aufmachung):
Anhang 1 - Übersicht aller bisher berichteten potentiellen Fälschungsverdachtsfälle in Deutschland
1) Bestätigte Fälschungen - CellCept 500 mg Filmtabletten Chargen (13)
Die Original Roche Aufmachung ist entweder nicht in Deutschland verkehrsfähig oder wurde nicht in der 150er Packungsgröße für den deutschen Markt zertifiziert.
Bestätigte Fälschung, 150er Packungsgröße, 3-Länderaufmachung (DE-NL-AT); Blister und Filmtablette entsprechen der Identität des Originalproduktes.
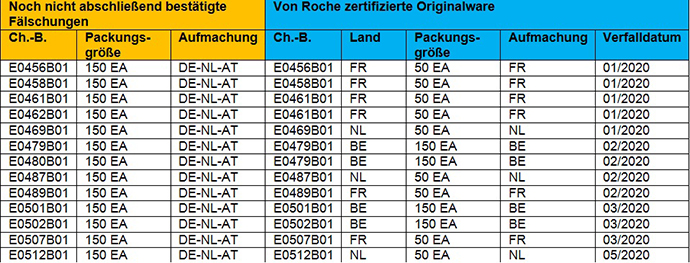
2) Noch nicht abschließend bestätigte Fälschungen - CellCept 500 mg Filmtabletten Chargen (13)
Die Original Roche Aufmachung ist entweder nicht in Deutschland verkehrsfähig oder wurde nicht in der 150er Packungsgröße für den deutschen Markt zertifiziert.
Reklamationsmuster befinden sich derzeit in Untersuchung.
Ergänzung vom 14.03.2018 (Chargen E0513B01, E0497B01)
Dem Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) liegen weitere Informationen zum Fälschungsfall des Arzneimittels CellCept® 500 mg Filmtabletten der Firma Roche Registration Limited vor. Für eine weitere Charge mit der Bezeichnung E0545B01 (Verfalldatum 04/2020) wurde der Fälschungsverdacht bestätigt. Die Charge ist eine real existierende Charge, die im Original in niederländischer Aufmachung für den niederländischen Markt bestimmt ist. Die Untersuchungen ergaben, dass bei den Fälschungen der Blister und die Tabletten Originalware sind, die Faltschachtel in deutsch-niederländisch-österreichischer Aufmachung mit den variablen Daten in lila Aufdruck hingegen gefälscht ist. Die Untersuchungen zu weiteren Chargen sind noch nicht abgeschlossen. Daher kann zum jetzigen Zeitpunkt nicht ausgeschlossen werden, dass noch weitere Chargen betroffen sind.
Ergänzung vom 06.03.2018 (Chargen E0513B01, E0497B01)
Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) weist auf Fälschungen des Arzneimittels CellCept® 500 mg Filmtabletten der Firma Roche Registration Limited hin, die in Deutschland in Apotheken und bei Großhändlern entdeckt wurden. Das Arzneimittel enthält regulär den Wirkstoff Mycophenolatmofetil und wird in Kombination mit Ciclosporin und Corticosteroiden zur Prophylaxe von akuten Transplantatabstoßungsreaktionen bei Patienten mit allogener Nieren-, Herz- oder Lebertransplantation angewendet. Gefälschte Arzneimittel wurden mit den Chargen-Bezeichnungen E0513B01 (Verfalldatum 03/2020) und E0497B01 (Verfalldatum 02/2020) identifiziert. Beide Chargen sind real existierende Chargen. Die Charge mit der Bezeichnung E0513B01 (Verfalldatum 03/2020) ist eine real existierende Charge, die im Original in norwegischer Aufmachung für den norwegischen Markt bestimmt ist. Die Charge mit der Bezeichnung E0497B01 (Verfalldatum 02/2020) ist eine real existierende Charge, die im Original in französischer Aufmachung für den französischen Markt bestimmt ist. Beide Chargen wurden illegal umverpackt und sind in deutsch-niederländisch-österreichischer Aufmachung auf den deutschen Markt gebracht worden. Untersuchungen der Firma Roche ergaben, dass die deutsch-niederländisch-österreichischen Faltschachteln in beiden Fällen gefälscht sind. Für beide Chargen (E0513B01 und E0497B01) wurde festgestellt, dass die Blister und Filmtabletten Originalware sind. Die Fälschungen sind anhand eines eindeutigen Kriteriums, der Druckfarbe der variablen Daten auf den Faltschachteln (Fälschung lila, Original schwarz), zu identifizieren (siehe Abbildungen). Die Untersuchungen sind in diesem Fall noch nicht abgeschlossen. Es kann daher nicht ausgeschlossen werden, dass noch weitere Chargen betroffen sind. Die Herkunft der Fälschungen wird untersucht. Sicher ist, dass die Fälschungen auf den deutschen Markt gelangt sind. Das BfArM steht in engem Kontakt mit den Landesbehörden, die in Deutschland für die Überwachung des Verkehrs mit Arzneimitteln zuständig sind, und der Europäischen Arzneimittelbehörde EMA. Sobald weitere Informationen vorliegen, wird das BfArM unverzüglich darüber informieren. Das BfArM weist Großhändler, Apotheker und Anwender darauf hin, die Farbe des Aufdrucks der Faltschachtel sowohl bei diesen, wie auch bei anderen Chargen des Arzneimittels zu prüfen und Verdachtsfälle dem BfArM zu melden. Fotos der Fälschungen in deutsch-niederländisch-österreichischer Aufmachung und des Originalproduktes (norwegische bzw. französische Aufmachung):
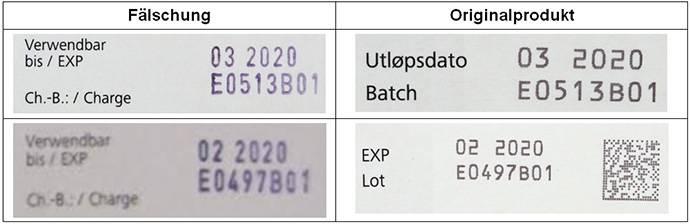
Mitteilung vom 28.02.2018 (Chargen E0513B01, E0497B01)
Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) weist auf Fälschungen des Arzneimittels CellCept® 500 mg Filmtabletten der Firma Roche Registration Limited hin, die in Deutschland in Apotheken und bei Großhändlern entdeckt wurden. Das Arzneimittel enthält regulär den Wirkstoff Mycophenolatmofetil und wird in Kombination mit Ciclosporin und Corticosteroiden zur Prophylaxe von akuten Transplantatabstoßungsreaktionen bei Patienten mit allogener Nieren-, Herz- oder Lebertransplantation angewendet. Die eine gefälschte Charge trägt die Bezeichnung E0513B01 (Verfalldatum 03/2020) und ist eine real existierende Charge in norwegischer Aufmachung für den Markt in Norwegen. Eine weitere gefälschte Charge trägt die Bezeichnung E0497B01 (Verfalldatum 02/2020) und ist eine real existierende Charge in französischer Aufmachung für den Markt in Frankreich. Beide Chargen wurden illegal umverpackt und sind dann in deutsch-niederländisch-österreichischer Aufmachung auf den deutschen Markt gebracht worden. Untersuchungen der Firma Roche ergaben, dass die deutsch-niederländisch-österreichischen Faltschachteln in beiden Fällen gefälscht sind. Für die Charge E0513B01 wurde festgestellt, dass die Blister und Filmtabletten Originalware sind. Für die Charge E0497B01 liegt noch kein Untersuchungsergebnis zu den Blistern und Filmtabletten vor. Die Fälschungen sind anhand eines eindeutigen Kriteriums, der Druckfarbe der variablen Daten auf den Faltschachteln (Fälschung lila, Original schwarz), zu identifizieren (siehe Abbildungen). Das BfArM weist Großhändler, Apotheker und Anwender darauf hin, die Farbe des Aufdrucks der Faltschachtel zu prüfen und Verdachtsfälle dem BfArM zu melden. Fotos der Fälschungen in deutsch-niederländisch-österreichischer Aufmachung und des Originalproduktes (norwegische bzw. französische Aufmachung):